Veľkou prednosťou NMR je, že v skupine látok rovnakého typu (v homologickom rade látok), ktoré sa líšia len variáciou určitej časti štruktúry (substituentom) možno variáciu chemických posunov so zmenou substituenta pomerne spoľahlivo určiť bez nutnosti použitia databáz, resp. programov na predikciu NMR spektier a to na základe polárneho efektu substituenta. Je to veľmi podobne ako pri posudzovaní vplyvu substituenta na reaktivitu organických látok pretože NMR chemické posuny i reaktivita reakčných centier závisia veľmi podobným spôsobom od elektrónovej hustoty v ich okolí. Na posúdenie vplyvu substituentov na NMR chemické posuny nám preto stačia základné vedomosti z organickej chémie pri posudzovaní vplyvu elektrónovej štruktúry na reaktivitu látok. Elektrónová hustota v okolí spinov je najdôležitejším faktorom vplývajúcim na hodnotu chemického posunu a z tohto dôvodu je jednoduchý koncept polárneho efektu dobre funkčný a spoľahlivý.
Efekt substituenta sa posudzuje ako zmena chemického posunu určitého jadra pri zámene vodíka za substituent. Efekt závisí od vzdialenosti (vyjadrenej počtom väzieb) medzi substituentom a daným jadrom. Obvykle s počtom väzieb efekt substituenta klesá. Podľa spôsobu prenosu možno efekt substituenta rozlíšiť na indukčný a mezomérny, ktorý sa prenáša cez π-elektrónový systém.
Indukčný efekt je spôsobený inou (obvykle vyššou) elektronegativitou substituentov oproti elektronegativite referenčného substituenta – vodíka. Prenáša cez σ-väzby a so vzdialenosťou klesá ako je to pre 13C chemické posuny naznačené na nasledujúcom obrázku.
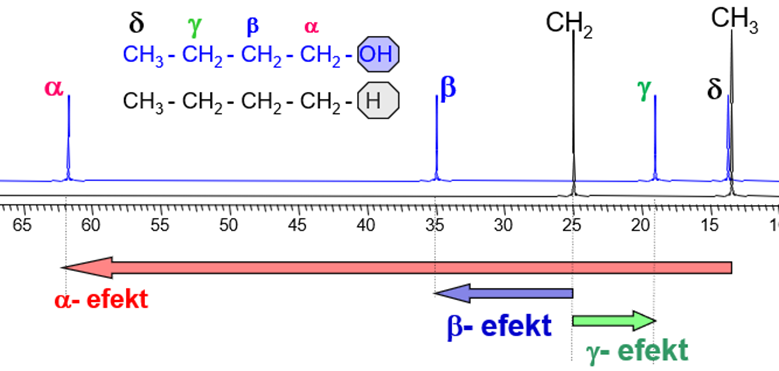
V tabuľke na obrázku č.35 je ukázaný efekt rôznych substituentov na 13C chemické posuny v n-alkánových a izo-alkánových skeletoch. Efekt substituenta je najvýraznejší v α-polohe vedľa substituenta a následne v β-polohe a γ-polohe. V δ-polohe je efekt obvykle veľmi malý, zanedbateľný a preto sa v tabuľkách neuvádza.
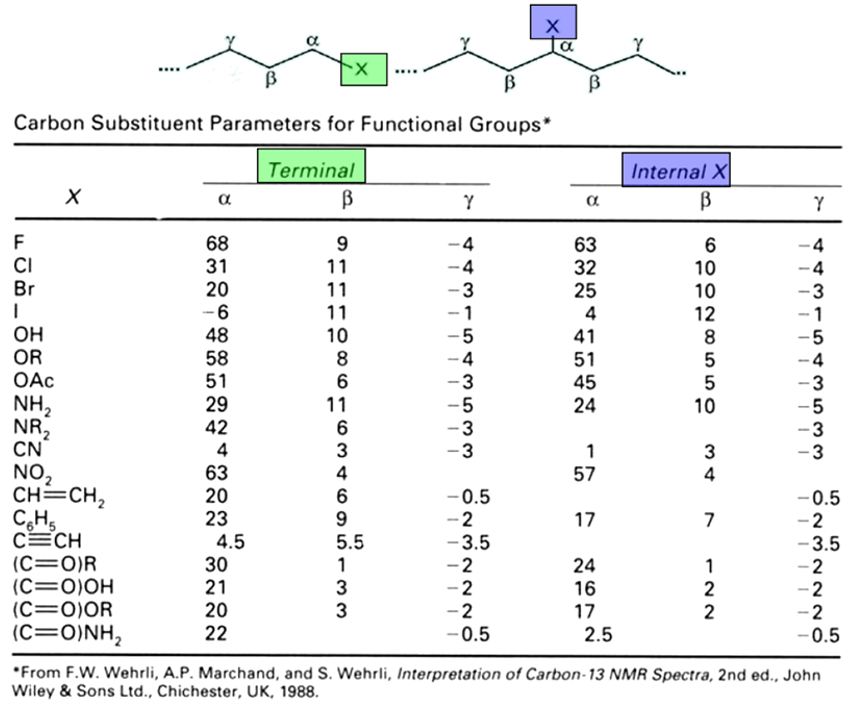
Podľa predpokladu elektronegatívny substituent znižuje elektrónovú hustotu v susedných polohách, čo sa prejaví zvýšením chemických posunov v α-polohe a β polohe (okrem jódu, ktorý svojim objemom silne znižuje lokálny paramagnetický efekt p-elektrónov na Cα ). Na prvý pohľad prekvapením je opačné znamienko γ-efektu. Doposiaľ nie je v literatúre dostupné jednoznačné vysvetlenie tejto skutočnosti. Najčastejšie sa to vysvetľuje ako dôsledok stérickej interakcie medzi vodíkom v γ-polohe a substituentom. Zaujímavosťou γ-efektu je, že je stereošpecifický: jeho absolútna hodnota je väčšia (viac negatívna) v tzv. γ-syn konfigurácií ako v γ-anti konfigurácii (pozri obr.36). Túto skutočnosť možno využiť pri určovaní relatívnej konfigurácie väzieb v analyzovanej štruktúre.
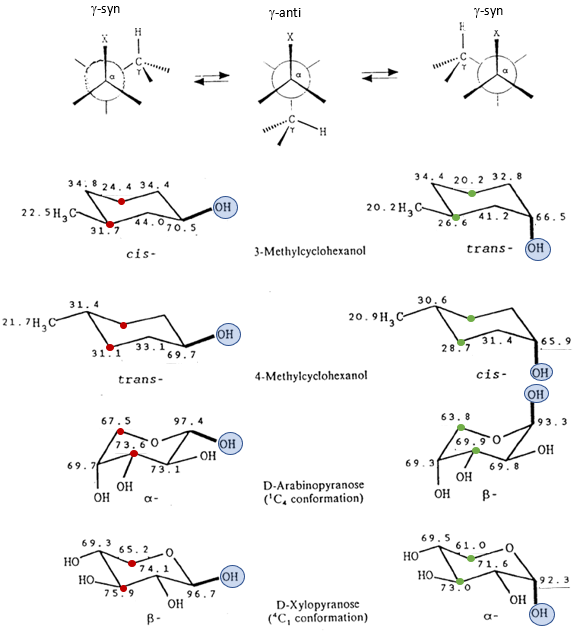
Čo sa týka efektu substituentov na 1H NMR chemické posuny v α a β polohe je podobný (zvyšovanie chemického posunu), ale oveľa menší ako efekt na 13C chemické posuny. V γ polohe je obvykle zanedbateľný.
Efekt substituentov sa podobným spôsobom ako na alkánoch prejavuje aj na iných štruktúrach. Podobné tabuľky ako je tabuľka uvedená na obr. 35 možno v literatúre nájsť aj pre iné homologické rady zlúčenín.
Problém 5. Na základe vyhodnotenia efektu substituenta priraďte signály v karbonylovej skupiny 13C NMR spektre zmesi ketónov: CH3COCH3, CH3CH2COCH3, CH3CH2CH2CH2COCH3, CH3CH2COCH(CH3)2 a CH3CH2CH(CH3)COCH3. (Nápoveda: porovnajte počet príspevkov substituentov v α, β a γ polohe ku karbonylovej skupiny pre každý ketón).
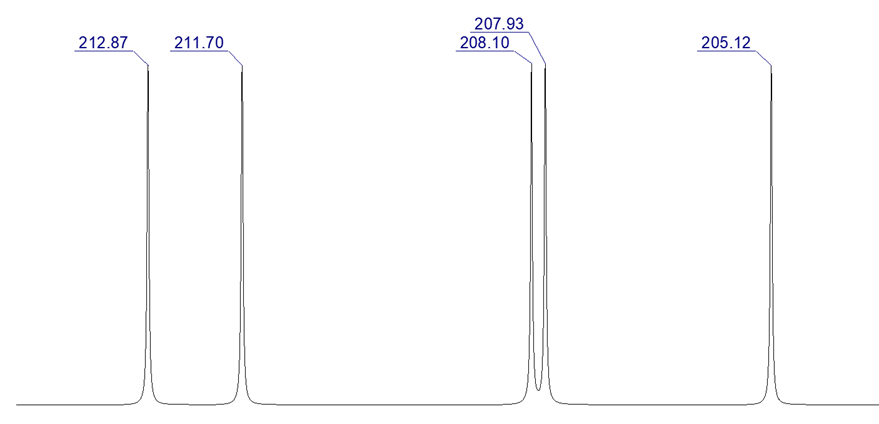
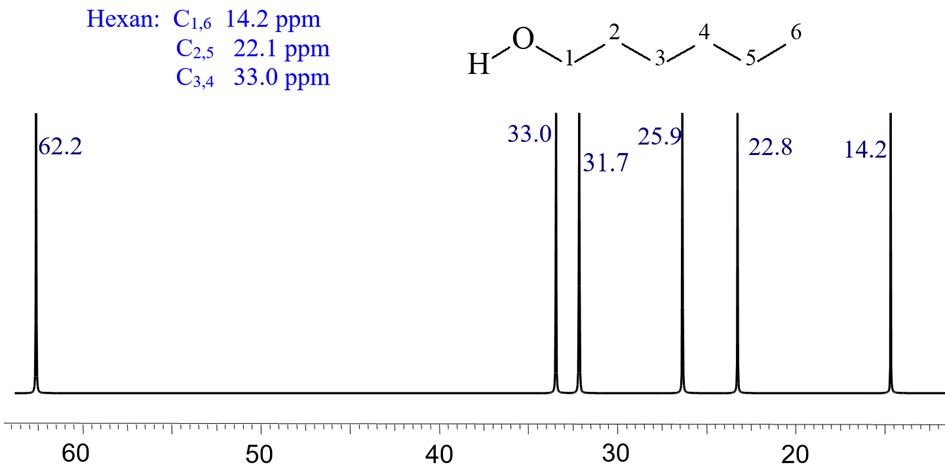
Problém 6. Na základe vyhodnotenia efektu substituenta priraďte signály v 13C NMR spektre 1-hexanolu
Mezomérny efekt sa prenáša π-elektrónmi v konjugovanom systéme násobných väzieb ako je to naznačené pre systém na aromatickom jadre na obr.35. Elektróno-donorné substituenty (–O− > –NH2 > –OR > –NHCOR > –OCOR > –Ph > –CH3 > –I > –Br > –Cl > –F ) zahusťujú elektrónovú hustotu v polohách orto a para vzhľadom k substituentu. Znamená to zvyšovanie tienenia v týchto polohách čo súčasne znamená aj znižovanie 1H a 13C chemických posunov. Naopak, elektróno-akceptórné substituenty (–NO2 > –CN > –SO3H > –CHO > –COR > –COOR > –COOH > –CONH2 > –COO−) v týchto polohách zrieďujú elektrónovú hustotu, a teda spôsobujú zvyšovanie 1H a 13C chemických posunov. Chemický posun v meta polohe je mezomérnym efektom ovplyvňovaný veľmi málo.
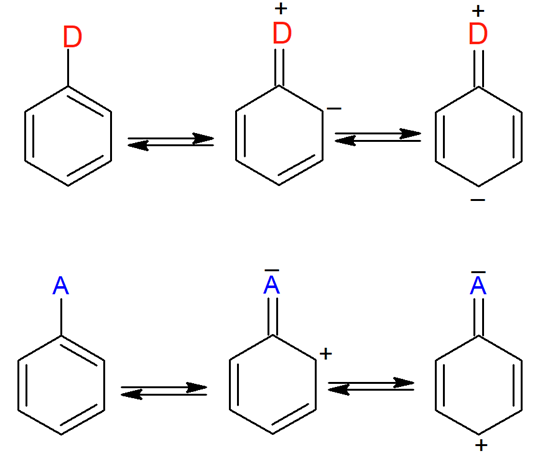
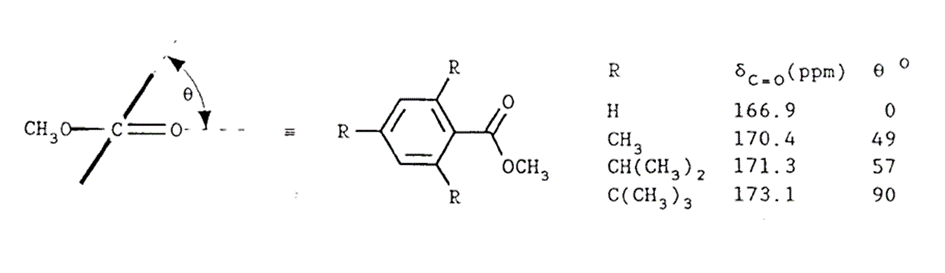
Mezomérny efekt je úplne nezávislý od indukčného efektu substituenta, a preto v polohách blízko substituenta (ipso a orto na aromatickom jadre), je potrebné uvažovať aj indukčný efekt. Celkový efekt v aromatických systémoch vystihujú empirické konštanty, v ktorých sú oba efekty zohľadnené (obr.38).
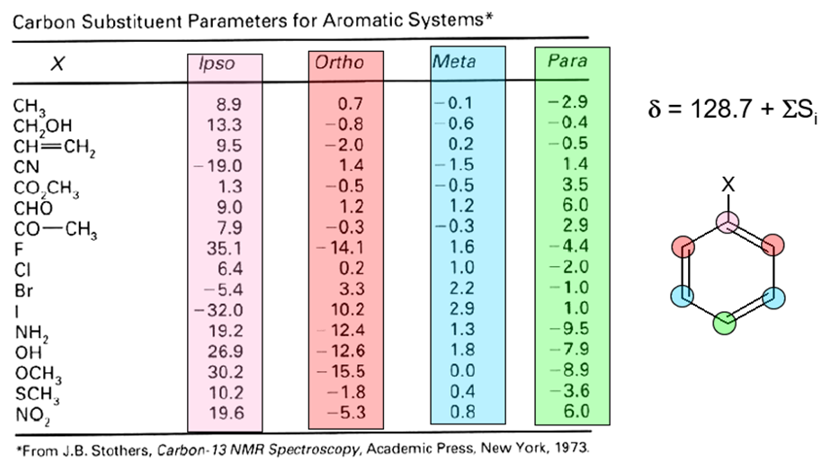
Podrobnejší pohľad na parametre substituentov však naznačuje, že vyššie uvedené jednoduché pravidla pre interpretáciu polárneho efektu substituentov platia dobre iba pre meta a para polohy. V ipso a orto polohách v prípade silných elektróno-akceptorných (NO2, CN) ako aj objemných (I, Br) substituentov je ich polárny efekt iný ako predpokladaný. Vysvetlením môže byť, že lokálny paramagnetický príspevok k 13C chemickému posunu uhlíkov (stupeň HOMO -> LUMO excitácie p-elektrónov) je v dôsledku stérického efektu týchto substituentov významne zmenšený.
Problém 7. Vysvetlite zmenu chemického posunu karbonylovej skupiny so zmenou veľkosti substituenta R.